| 8.2.3 Biologické účinky |
Absorpce elektromagnetického záření
Grotthus-Draperovův zákon říká, že k jakékoliv fotochemické reakci může dojít pouze tehdy, jestliže je dopadající záření absorbováno molekulami jemu vystavené látky, přičemž se mění elektromagnetická energie na energii chemickou. Těmito molekulami jsou zpravidla molekuly DNA, RNA, bílkovin, porfyrinů a dalších sloučenin. Absorpce fotonů excituje molekulu ozářené sloučeniny na vyšší energetickou hladinu, například v excitovaný singletový stav. Vzhledem k energii, požadované pro přesun molekul na vyšší hladinu a pro vyvolání vibračního a rotačního pohybu jejich jader, je každá chemická sloučenina schopna absorbovat záření pouze určitých vlnových délek. Molekuly zůstávají ve svém excitovaném stavu do doby, než se sloučenina chemicky změní ve fotoprodukt, který přenese energii na další molekulu, nebo ji vyzáří jako energii světelnou či tepelnou. Přenosem energie může být podmíněn vznik morfologické reakce s navozením různých biochemických pochodů, například indukce nebo inaktivace enzymů, vznik iontových stavů, replikace DNA apod. Ty posléze vedou k buněčným změnám - proliferačním, mutagenním, toxickým a dalším. U každé sloučeniny závisí pravděpodobnost absorpce elektromagnetického záření kromě jeho intenzity na vlnové délce. O vlnové délce s nejvyšší absorpční schopností se hovoří jako o absorpčním maximu. Absorpční spektrum je přitom různé u každé molekulární struktury každé sloučeniny.
Aplikace terapeutického laseru
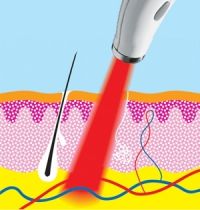
Nejvýznamnější absorpční struktury pro infračervené vlnové délky laserů používané při LLLT jsou dle studií proteiny, nicméně přesný fotoreceptor odpovědný za biologický efekt zatím není přesně identifikován. Některé studie se kloní spíše k mitochondriálním cytochromům nebo endogenním porfyrinům buňky, jako k chromoforům absorbujícím energii. Při průniku laserového záření do tkání dochází mimo jiné k rozptylu energie erytrocyty v kapilárách. Interakce laserového záření s tkáníÚčinky laserového záření závisí na reflektanci záření (odražená zářivá energie v procentech rozptylu záření tkání a zpětném odrazu částicemi (molekulami, organelami), remitanci (zpětný odraz na povrch), difůzi a transmisi paprsků v biologickém prostředí a na absorpci. Absorbovaná světelná laserová energie fotonů se začleňuje do energetických procesů v ozářené tkáni a to podle dosažených hodnot hustoty energie a podle doby působení, ve které je tato energie přiváděna.
Terapeutický účinek laseru
Fotochemické účinky laseruAbsorbovaná energie fotonů laserového záření může zasahovat do chemických procesů nejrůznějšími mechanizmy. Po transmisi paprsku tuto energii nejprve hodnotí buňka cílové tkáně a přenáší ji jako informaci na buňky jiné nebo od nitra buňky a dalšími mechanismy přenosu se dostává informace k mitochondriím, kde se dějí vlastní biochemické procesy. Fotochemické účinky laserového záření jsou založeny na principu absorpce jednotlivých fotonů, které vyvolávají biochemické pochody. Takovéto reakce mohou probíhat již při malých intenzitách.
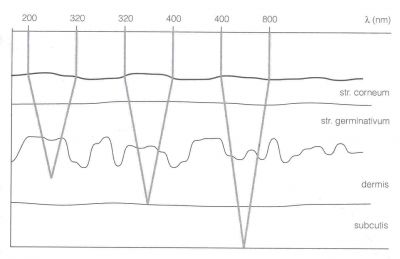
Hloubka průniku světla do kůže v závislosti na vlnové délce
Účinek terapeutického laseru na celulární úrovniMechanismus biologických účinků nízkovýkonných laserů je ověřován in vitro i in vivo. Je popisován stimulační, protizánětlivý i analgetický efekt. Stimulační efekt aktivuje enzymy dýchacího řetězce (flavin dehydrogenázu, cytochromoxidázu) v mitochondriích. Enzymy se účastní oxidační reakce (přenos elektronu ze substrátů na kyslík), jejímž výsledkem je tvorba ATP. Zvýšená koncentrace ATP, ADP a AMP, při laserem navozeném stimulačním efektu, vede k replikaci mitochondriální DNA. Výsledkem je urychlená epitelizace postižené tkáně a stimulace tvorby kolagenu. Při protizánětlivém účinku nízkovýkonný laser aktivuje přirozené reparační procesy, kterými organismus reaguje na probíhající zánět. Zvyšuje se chemotaktická aktivita buněk (lymfocytů, monocytů, fibroblastů a polymorfonukleárních buněk), které se na protizánětlivé reakci organismu podílí.
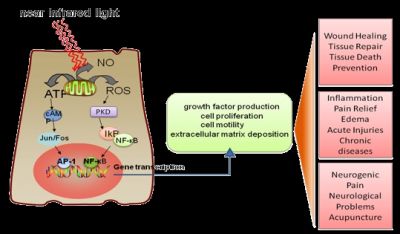
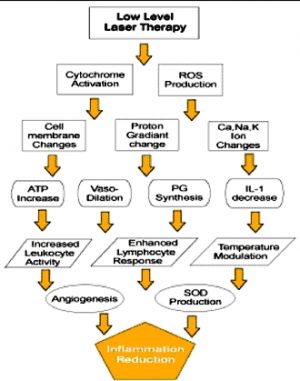
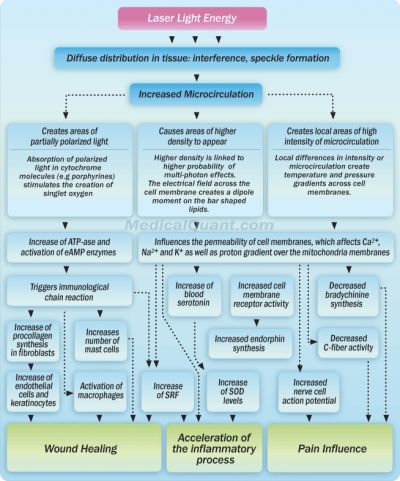
Mechanismus účinku terapeutického laseru
Dalším z důsledků působení nízkovýkonného laseru je zvýšená mikrocirkulace v ozářeném organismu, k čemuž dochází díky zvýšenému tkáňovému metabolismu. Podpořena je proliferace fibroblastů a tvorba kolagenových vláken, které se orientují paralelně a vytváří jizvu. Jedna z reakcí při analgetickém účinku je uvolnění endogenních opiátů. Ty se pak navážou na opiátové receptory nociceptivního systému. Při absorpci laserového záření dochází na molekulární úrovni k elektronovým přechodům. Typ přechodu je závislý na vlnové délce působícího záření. Při absorpci laserového záření v UV oblasti je navozen fotochemický jev. Elektrony přecházejí ze základní hladiny do excitovaných stavů, při zpětném přechodu na základní hladinu dochází k přenosu energie na substrát. U laserů vyzařujících v infračervené oblasti je navozen fototermický jev. Energie infračervených fotonů obvykle nedostačuje k iniciaci přechodů elektronů mezi hladinami; dochází pouze k stimulaci rotačně vibračních stavů molekul. Viditelné záření pak iniciuje jak reakci fotochemickou, tak i fototermickou.
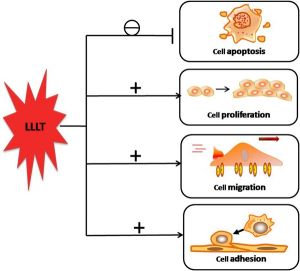
Buněčná odezva na ozáření terapeutickým laserem
Přenos mezibuněčné informacePřenos biologické a fyzikální informace na buňku je jedním z ústředních problémů molekulární biologie. Při zachycení informace ji buňka buď zpracuje a využije pro své funkce anebo ji částečně či úplně přenese na jinou buňku v rámci mezibuněčné komunikace. Buňka přijímá informaci z prostředí receptory na povrchu membrány, která je opatřena složenými jednak z bílkovinných struktur, jednak z polymerů cukrů, které mohou na jednotku hmoty unést více informací než bílkoviny, protože vytvářejí neobyčejné množství různých struktur. Rozvětvená síť membránových glykoproteinů dekóduje jazyk informace a rozhoduje o odpovědi - imunitní, mezibuněčné komunikaci, maligní přeměně nebo energetické spotřebě. Zachycená a dekódovaná informace strukturami buněčné membrány je přenášena dovnitř buňky. K přenosu jsou vhodné malé molekuly, které snadno membránou proniknou a nevyžadují příliš specifický a složitý systém. Těchto transmiterů je objevena již celá řada, např. molekula oxidu dusnatého (NO). Klíčovou úlohu při nitrobuněčné komunikaci mezi receptory a efektory hrají tzv. G-proteiny. Jejich úkolem je zprostředkovat a přenášet signál z různých signálních molekul na příslušný efektor uvnitř buňky. G-proteiny jsou uloženy na vnitřní straně buněčné membrány a po své aktivaci se začnou pohybovat k dalšímu efektoru - bílkovině, která po své aktivaci začne vyrábět druhého posla - cyklický adenosinmonofosfát (cAMP), který díky své zvláštní chemické struktuře vyvolává řadu chemických reakcí. Četné metabolické a regulační pochody v buňkách jsou řízeny podle informací, které získávají z vnějšího prostoru, mezibuněčného prostoru a od jiných buněk z okolí nebo buněk vzdálených. Výsledkem jsou nejrůznější biochemické účinky zajišťované modifikacemi četných enzymatických reakcí, které vedou ke stimulaci nebo inhibici struktur.
Terapeutický laser
Protizánětlivý účinek laseruZánět je složitou komplexní reakcí na nejrůznější noxy, mikroorganismy, traumata, kalorické a chemické činitele, imunologické reakce atd. Terapeutický laser aktivuje při cílené aplikaci přirozené protizánětlivé procesy, kterými organizmus na probíhající zánět reaguje. Buňky zánětlivé tkáně produkují histamin, bradykinin, serotonin, zvyšuje se lokální prokrvení a permeabilita cév, takže dochází k přesunu proteinů a tekutiny z intravazálního prostoru do intersticia a vzniku otoku. Tužší elastický otok v zánětlivé tkáni se formuje po transportu krevního proteinu fibrinogenu, změnou fibrinogenu na fibrin a koagulací fibrinu vedoucí k oblenění tkáně a lymfatické tekutiny - tento proces izoluje postiženou tkáň od zdravého okolí.
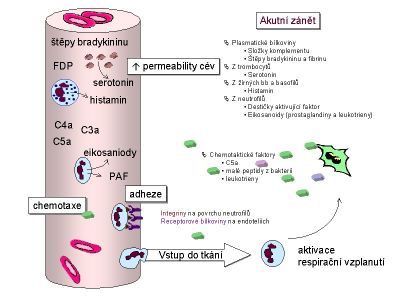
Akutní zánětlivá odpověď
Obranné mechanizmy nastupují rychle. Nejprve se mobilizují neutrofilní granulocyty, které jsou schopny fagocytovat cizí elementy, uvolňují se substance zvyšující neutrofilní leukocyty v krvi, které pak dosahují k zánětlivé oblasti marginací, diapedezí a chemotaxí. Progresivně se zvyšuje počet neutrofilních granulocytů a produkce monocytů v kostní dřeni.
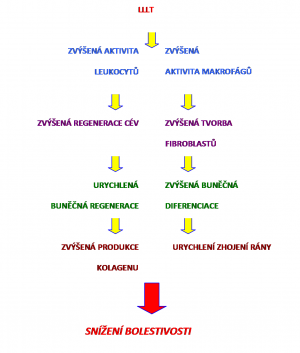
Schéma protizánětlivého účinku terapeutického laseru
Laser má v celém procesu významný terapeutický efekt na zánětlivou symptomatologii, tj. na otok, bolest, zarudnutí i zvýšenou teplotu. I těžké záněty lze od začátku ozařovat laserem, jehož stimulace fagocytózy byla opakovaně prokázána. Neutrofilní leukocyty a mikrofágy při fagocytóze emitují světlo ve vlnových délkách červených a infračervených. Reaktivní kyslík z oxidativního metabolizmu fagocytů je účinný pro stimulaci membrány fagocytů a dokáže značně rozrušovat četné mikroorganismy. Důležitým činitelem těchto reaktivních kyslíkových složek je instabilita, vedoucí k světelné emisi, což bylo nazváno chemoluminiscencí.
Aplikace terapeutického laseru na oblast paty a páteře
Analgetický účinek terapeutického laseruVedle mechanizmů periferního systému receptorů a drah, vedoucích nocicepční podněty, jsou k dispozici také mechanizmy nocicepčních receptorů v centrálním nervovém systému, které souvisejí s tvorbou neurotransmiterů, enkefalinů a endorfinů. Skupina endogenních látek, podobných opiátům, se tvoří z peptidů s řetězci aminokyselin různé délky. Jejich základem je H-tyrosin-glycin-fenylalanin a liší se poslední složkou methioninem-OH nebo leucinem (enkefaliny, endorfiny) -OH. Mají silnou vazbu na opiátové receptory. Jejich fyziologický význam je ve funkci neurotransmiterů, spíše neuromodulátorů, které zajišťují sympatický přenos vzruchů mezi neurony. Přesný mechanismus analgetického účinku není znám. Jedna z reakcí, která se při něm uplatňuje, je uvolnění endogenních opiátů. Ty se pak navážou na opiátové receptory nociceptivního systému. Na molekulární úrovni při absorpci laserového záření dochází k elektronovým přechodům. Typ přechodu je závislý na vlnové délce působícího záření. Při absorpci laserového záření v UV oblasti je navozen fotochemický jev. Elektrony přecházejí ze základní hladiny do excitovaných stavů, při zpětném přechodu na základní hladinu dochází k přenosu energie na substrát. U laserů vyzařujících v infračervené oblasti je navozen při absorpci fototermický jev. Energie infračervených fotonů obvykle nedostačuje k iniciaci přechodů elektronů mezi hladinami; dochází pouze k stimulaci rotačně vibračních stavů molekul. Viditelné záření pak iniciuje jak reakci fotochemickou, tak i fototermickou. Laser také zřejmě ovlivňuje uvolňování endogenních opiátů, které se váží na opiátové receptory nociceptivního systému a především substantia grisea centralis (PAG), který je jimi na mnoha místech obsazen a tak je rovněž dosaženo žádoucího analgetického efektu. Tento poznatek podporují práce popisující po lokální aplikaci laseru nárůst sekrece kyseliny 5-hydroxyindoloctové (produktu degradace serotoninu) v moči a to zvláště u lidí s chronickou bolestí.
Stimulační účinek laseruLaser, který je reprezentován energií fotonů, má důležitý vliv na enzymatické reakce a to ve smyslu stimulace. Ovlivněním enzymatických reakcí dochází ke zvýšené syntéze ATP, zatímco spotřeba glukózy se snižuje. Tento makroergní fosfát je dále zdrojem energie, který může využívat buňka k jiným biochemickým syntézám. Tato přeměna ADP na ATP se děje na mitochondiích v rámci oxidativní fosforylace - v rámci dýchacího řetězce. Zvýšení energetického potenciálu má zejména význam u buněk postižených patologickým procesem, kdy tyto buňky trpí deficitem energie. Podobně buňky, které jsou ve fázi hojení, mají vysokou spotřebu ATP, neboť i tento reparační proces je spojen s velkou spotřebou energie. Pokud se stimulují laserem buňky zdravé, které nepotřebují produkci ATP, pak tento nadbytek ATP se nepřeměňuje v tepelnou energii, jak se původně soudilo, ale převádí se energie fotonů jako forma světelné energie k jiným buňkám, které vykazují při produkci ATP energetický deficit. Laserovým zářením stimulované buněčné dýchání urychlí některé metabolické reakce buňky, zvýší imunologické reakce a podporuje zejména mitózu buněk. Lasery se svými paprsky podílejí i na fibrinolytické aktivitě.
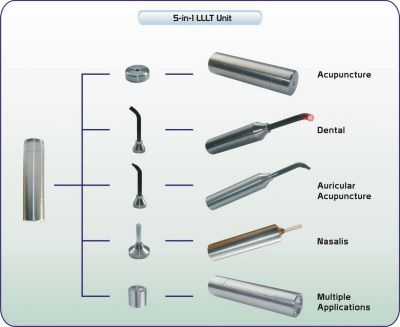
Typy sond k laserové terapii
Série pro laseroterapii
Stimulace hojení ranPříznivé výsledky byly získány i v klinické praxi při léčbě ran a chronických zánětů nízkovýkonným laserem. Oba tyto patologické stavy jsou charakterizované sníženou tenzí kyslíku a následnou acidózou. V případě regenerace tkáně je hypoxie v oblasti rány stavem pouze přechodným. Jiná je ale situace u chronických zánětů, kdy nastává kontinuální aerobní glykolýza a redukční posun směrem ve směru snížení. Jsou-li ozářeny časné rány, účinek laseru může být minimální až nulový a to i v případě, kdy je proliferace aktivní a regenerace integrity tkáně probíhá v podstatě maximálním tempem (fyziologicky).
Přenosný terapeutický laser
Schéma stimulačního účinku laseru
|